缺氧环境(例如管道内部)中的铁(Fe0)腐蚀是一个涉及相当大经济成本的过程,该过程很大程度上受微生物影响,特别是硫酸盐还原菌(SRB)。该过程的特点是形成黑色结壳和金属点蚀。该机制通常用形成的H2S 的腐蚀性来解释,以及从Fe0与H2O的化学反应中清除“阴极”H2。在这里,我们研究了以金属铁作为唯一电子供体进行化能自养生长的特殊海洋SRB。它们在五个月内降解了高达 72%的铁片(10 mm × 10 mm × 1 mm),这是一个技术高度相关的腐蚀速率(0.7 mm Fe0/年),而传统的H2清除控制菌株没有腐蚀性。在腐蚀金属上沉积的黑色、坚硬的矿物结壳(FeS、FeCO3、Mg/CaCO3)表现出电导率(50 S m−1)。 这足以解释金属通过半导体硫化物向结壳定殖细胞传递电子(4Fe0 → 4Fe2+ + 8e−)的腐蚀速率,而细胞则还原硫酸盐(8e− + SO42− + 9H+ → HS− + 4H2O)。因此,厌氧微生物铁腐蚀显然绕过了H2,而非依赖它。具有这种腐蚀潜力的硫酸盐还原菌在沿海海洋沉积物位点以自然高数量被发现。埋藏在那里的铁片被腐蚀并覆盖了特征性的矿物结壳。据推测,厌氧生物腐蚀是由于生态生理学相关的分解特性被混杂使用,用于从沉积物中的非生物或生物来源获取外部电子。
硫酸盐还原菌(SRB)可以通过一种与CMIC 根本不同的机制,更深入地参与厌氧铁腐蚀。这一观点最早在一项开创性的研究中被提出,该研究研究了缺氧土壤中的铁管腐蚀(von Wolzogen Kühr 和 van der Vlugt, 1934)。研究表明,SRB 将铁作为硫酸盐还原的唯一还原当量来源。这种纯粹化能自养过程的净化学计量,此处与常见的碳酸盐(菱铁矿)沉淀一起,是:
然而,这种总方程并不能提供关于从铁到硫酸盐还原的还原当量传递的实际形式的线索。考虑 H2(来自 H2O 还原)作为中间体(Booth 和 Tiller, 1960; von Wolzogen Kühr, 1961; Bryant 和 Laishley, 1990; Coetser 和 Cloete, 2005)具有吸引力,实际上它是许多硫酸盐还原菌的优良生长底物。它们的高亲和力氢捕获(4H2 + SO42− + 2H+ → H2S + 4H2O)被认为会“拉动”初级氧化(von Wolzogen Kühr 和 van der Vlugt, 1934; von Wolzogen Kühr, 1961),这也是教科书中的常见解释。另一方面,由于H2的利用导致的厌氧腐蚀加速受到了批判(Costello, 1974; Hardy, 1983)。在几项动力学研究中,氢捕获并没有加速铁的氧化(Spruit 和 Wanklyn, 1951; Dinh 等 ., 2004; Mori 等 ., 2010)。 此外,新发现的海洋δ-变形菌纲硫酸盐还原菌(SRB)在直接以金属铁作为唯一电子供体进行富集和分离时,其硫酸盐的还原速度远快于单纯通过清除H2所能达到的速度,并且其腐蚀性比传统菌株更强(Dinh et al., 2004)。此外,它们会暂时产生大量H2而不是清除它,这可能是由于初始时铁衍生的还原能量过剩。因此,假设它们能够比通过缓慢形成的非生物H2更有效地利用 Fe0 进行硫酸盐呼吸,即通过更快的旁路途径,并且已经提出了直接从铁中获取电子的假说(Dinh et al., 2004)。这一理论在此被称为“电微生物影响腐蚀”(EMIC)。
在本研究中,我们详细研究了这些硫酸盐还原菌菌株对铁的破坏程度,以及假定的 EMIC 及其意义。首先,我们测量了在适当调整的培养条件下,是否也能达到工业环境中观察到的腐蚀速率。其次,我们考察了无机黑色腐蚀层(Dinh et al., 2004)对金属基底的覆盖程度是否与逐渐腐蚀和假设的金属电子摄取相兼容。第三,我们在自然海洋沉积物中埋藏铁样,以证明现场腐蚀现象是否与实验室培养实验中观察到的现象相似。
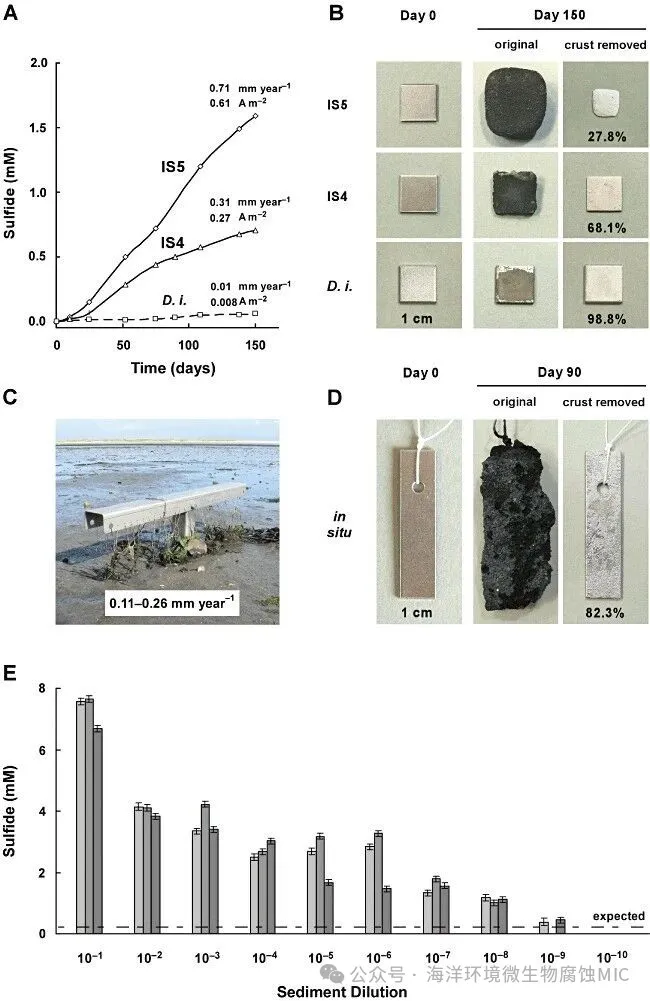
图一:纯培养和原位腐蚀性硫酸盐还原菌。A. 腐蚀菌株 IS5 和 IS4(分别提出:Desulfovibrio ferrophilus 和 Desulfopila corrodens)培养中长期硫化物形成(以硫酸盐消耗量衡量),铁片作为唯一的电子供体,以及氢营养对照培养(Desulfopila inferna, D. i.)。B. 相同培养中的厚腐蚀层和金属损失。去除腐蚀层后,残留金属(初始百分比)在用 HCl-六胺处理后变得明显。C. 沃登海,Sylt 岛(北海)中铁片的定位装置(不锈钢)。铁片用线绑在装置上,埋在缺氧沉积物中≥20 厘米深处三个月。D. 腐蚀层(含沙粒)和腐蚀金属(腐蚀层溶解后)来自(C)。此处拍摄的新鲜铁片(第 0 天)与培养的铁片不同。E. 六个月后,在原位沉积物(2 克,湿重)中进行系列稀释(平行三组)后形成的硫化物(以硫酸盐消耗量衡量)。 这条线表示仅通过铁和海水形成的氢气(H2)消耗所预期的硫化物(基于独立测量的氢气形成速率和仅使用氢气清除 SRB 的实验)。
金属铁是一种非常紧凑、致密的电子供体形式,足以将相对较大的培养体积中的溶解硫酸盐还原。在初始研究(Dinh et al., 2004)中,培养体积(0.15 升)与金属(30 克)的比例保持相对较小,以便在 20 天内清晰地揭示新型海洋硫酸盐还原菌的腐蚀潜力。在这样的培养过程中,硫酸盐还原速率一段时间后会显著减慢。在本研究的详细检查中表明,这种活性下降主要是由于明显的碱化和CO2(溶解和气态)的耗尽。对于旨在在更长时间的培养条件下,检测与现场条件下相当的铁破坏的生物腐蚀实验,培养(和气相)体积与金属质量的比例必须增加。由于宏观腐蚀现象是核心关注点,铁样品(10 毫米 × 10 毫米 × 1 毫米)不能进行任何程度的微型化,因此需要更大的培养体积。一个合适的培养基体积是 1.4 升,这个体积仍然足够进行硫酸盐消耗的精确监测。
实际上,腐蚀速率在数月内并没有显著下降。腐蚀性培养物的腐蚀速率高达 0.7 毫米铁0/年,并持续沉积不断增厚的黑色锈层( 图 1A 和 B)。在选择性去除锈层后,明显的金属损失现象可见( 图 1B)。在本实验中,菌株 IS5 的腐蚀性比菌株 IS4 更强,而在最初的生理特性表征(Dinh 等 ., 2004)中,后者腐蚀性更强。这可能是由于菌株 IS4 对先前培养中显著升高的 pH 值具有更高的耐受性。‘传统’硫酸盐还原菌(对照菌株),包括Desulfopila inferna(与菌株 IS4 系统发育相关的菌种;Gittel 等 ., 2010)和本研究中分离出的有效氢气清除剂 Desulfovibrio 菌株HS3,在培养期间基本没有显示铁腐蚀的迹象。这些对照培养中的铁受影响程度与无菌培养相当。 无法更有效地利用铁并非由于对Fe2+离子的敏感性。对照菌株能够清除由铁和水形成的H2( 公式 2),其浓度低于检测限(40 ppmv),并且当外部提供H2时,它们在铁的存在下能够顺利生长。
-
实际考虑
通过合金化或涂层来保护铁免受腐蚀在技术和经济上都不可能。例如,最重要的合金金属铬的产量比铁低 48 倍( 美国地质调查局,2011 年 ;2009 年数据)。因此,我们预计,对原位微生物诱导腐蚀(MIC)的分析和控制方面的进展仍将是一个相关议题。
一个长期目标是基于对导致微生物诱导腐蚀(MIC)的环境条件和机制的深入了解,设计特定的应对措施。这种“因果”方法面临着 MIC 中化学条件(例如电子受体或除金属铁外的电子供体的可用性)以及化学、电化学和微生物反应的复杂性。作者认为最有前景的研究策略是对单个和基本过程进行实验“剖析”,以便后续进行综述。在前面的研究(Dinh et al., 2004)和本研究中,我们专注于在严格缺氧条件下,以金属铁作为唯一电子供体,硫酸盐作为电子受体时的嗜石生物生长。此外,更全面的微生物学调查必须考虑硫酸盐有限时嗜石产甲烷古菌(Dinh et al., 2004; Mori et al., 2010; Uchiyama et al., 2010)或由于有机富集环境中硫酸盐还原菌(SRB)的有机营养生长导致的复合微生物诱导腐蚀(CMIC)对腐蚀的贡献。 在所涉及的这些无机化合物中,具有精细且多变的化学和电化学性质的硫化铁是核心研究对象。它们不仅可以介导电子流动。在特定的高硫条件下,硫化铁显然可以保护下方的金属免受进一步的快速腐蚀(Smith and Miller, 1975; Lee et al., 1995)。铁硫化物在间歇性缺氧-好氧条件下具有不同的作用,此时腐蚀可能特别严重。这主要可以用亚铁硫化物的化学氧化产物对铁的活性来解释(Jack, 2002; Hamilton, 2003; Beech and Sunner, 2007)。
鉴于目前对 MIC 原位情况的了解有限,控制措施的建议也受到限制。只要特定情况下的 MIC 主要是 CMIC,如果能识别并消除厌氧细菌的有机营养物,就可以进行预防。如果 MIC 本质上是 EMIC,避免含硫酸盐的水将是一个根本性的解决方案。扩展的体外和试点研究可能会阐明硝酸盐的添加在多大程度上也适用于控制 CMIC 和 EMIC——硝酸盐用于控制石油储层中生物生成的H2S(酸化)(Reinsel et al., 1996; Gieg et al., 2011),也可能有助于控制 CMIC 和 EMIC(Hubert et al., 2005; Schwermer et al., 2008)。
-
铁腐蚀能力的生理和生态意义
利用金属铁作为电子供体的特殊能力是一种生理学上引人注目的能力,其生态意义目前尚不清楚。除了少数情况(陨石、深部地表罕见的岩石;Deutsch 等 ,1977;Haggerty 和 Toft,1985),金属铁仅在工业化后才大规模进入环境,从进化角度来看,这可以说是非常“近期”的。然而,通过使用缺氧沉积物和金属铁进行稀释系列计数,发现腐蚀性硫酸盐还原菌数量为每克湿重数百万细胞,尽管明显缺乏人工铁结构。人们可以推测,腐蚀性代表了长期存在的生理特征的混杂利用,用于环境电子摄取(“电营养”;Lovley,2011),这种特征也适合利用人为引入的金属作为底物。通常,具有这种特征的硫酸盐还原菌可能参与通过硫化物海洋沉积物和其他生态系统的生物电子流(Nakamura 等 ,2009;Nielsen 等 。, 2010; Kato 等 ., 2011). 此外,电子获取也可能通过与具有过量催化电子的其他细菌直接接触(Summers 等 ., 2010; Lovley, 2011)或从强还原性、反应性矿物表面获得,例如由亚铁硫化物和游离硫化物形成的黄铁矿(FeS + H2S → FeS2 + H2 / FeS2 + 2H+ + 2e−; Wächtershäuser, 1992),这些可被视为直接腐蚀背后电子摄取系统的真正作用。总结了具有从外部来源获取电子能力的 SRB 的原位功能假说。这样的 SRB 可能代表迄今为止被忽视的厌氧群落的一部分。 然而,仍需对它们在各种自然地点的丰度进行更广泛的考察(如上述稀释系列)以及生理学研究,以揭示它们在厌氧矿物化中的真正意义。
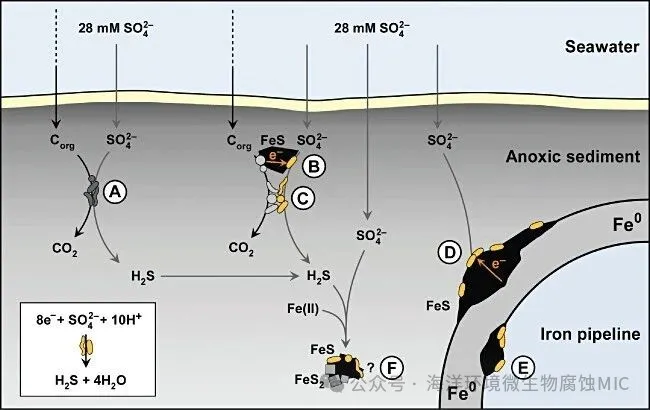
图二:目前关于能在缺氧海洋沉积物中从外部来源获取电子的硫酸盐还原菌(SRB)作用的综合假说(未按比例)。A. 传统的有机营养型 SRB。B. 通过导电性硫化亚铁与供电子有机营养厌氧微生物相互作用的 SRB。C. 直接接触供电子有机营养厌氧微生物的 SRB。D. 特殊 SRB 在管道外表面利用金属铁作为电子源。E. 特殊 SRB 在管道内部利用金属铁作为电子源。F. 硫铁矿化 FeS(FeS + H2S → FeS2 + 2H+ + 2e−)作为硫酸盐还原的直接电子源的推测可能性。
从机制演化的角度来看,仅涉及电子传递和接受的反应可以被视为简单甚至原始的。单纯的电子转移不需要额外的催化机制,例如 C-H 键(或 H-H 键)的断裂和结合原子的重排。对于许多简单的电子供体和受体,电子传递仅仅根据氧化还原电位发生,而不需要特定的催化。这是生物化学中的一个经典原理,例如,如果使用电子接受或供体染料(如紫精或六氰合铁酸盐)与非特异性氧化还原蛋白反应。在细胞中,作为电子传递载体的辅因子,即使在自由溶解状态下,也会因为非特异性的氧化还原反应而变得至关重要。它们的还原能力或氧化能力必须通过嵌入蛋白质(血红素、黄素)或限制在亲脂性的细胞膜(醌类)中来控制。仅仅接受或提供电子的物质在细胞外远不关键,而通过跨膜电子传递组分利用它们的能力显然是环境原核生物的一个典型领域。
总之,微生物腐蚀的研究除了具有明显的实际意义外,还包括有趣的机理、生态和进化方面。它可能成为“电微生物学”这一新兴领域中的第四个主题,除了微生物燃料电池(Lovley, 2006; Nealson and Finkel, 2011)、用于从水中制氢的微生物电解池(Croese et al., 2011)以及环境中的生物电流(Nakamura et al., 2009; Nielsen et al., 2010; Kato et al., 2011)之外,从而为未来的综合观点做出贡献。
免责声明:本网站所转载的文字、图片与视频资料版权归原创作者所有,如果涉及侵权,请第一时间联系本网删除。

官方微信
《腐蚀与防护网电子期刊》征订启事
- 投稿联系:编辑部
- 电话:010-62316606
- 邮箱:fsfhzy666@163.com
- 腐蚀与防护网官方QQ群:140808415