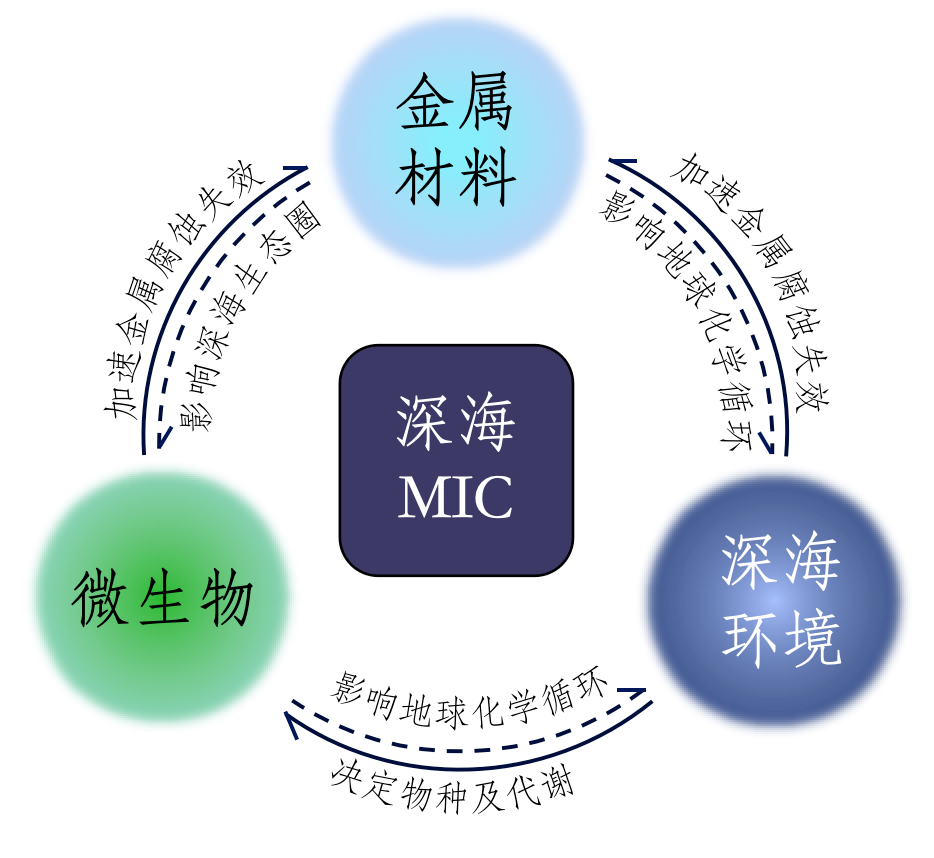
金属材料在海洋服役过程中普遍面临腐蚀风险,其中微生物腐蚀(microbiologically influenced corrosion,MIC)是导致材料失效的重要因素之一 [1]。MIC是指微生物通过其代谢活动及代谢产物影响金属表面的电化学过程,从而引发或加速腐蚀的现象[2]。MIC的研究可追溯至20世纪上半叶,von Wolzogen Kuhr和van der Vlugt于1934年提出了著名的“阴极去极化理论”,认为硫酸盐还原菌(sulfate-reducing bacteria, SRB)可通过消耗阴极产生的氢气而加速铁腐蚀[3]。同期,ZoBell系统研究了海洋细菌的附着行为及其与金属界面的相互作用,为理解海洋环境中的微生物-金属界面过程奠定了基础[4]。此后,Dexter[5]在海水体系中系统揭示了生物膜对阴极极化及腐蚀行为的影响,明确了生物膜与电化学过程之间的耦合关系;Hamilton[6]则从微生物生理与生化反应角度系统总结了SRB引发金属腐蚀的主要机制。这些工作共同构成了现代MIC理论的早期基础。 随着对微生物-金属界面过程认识的不断深化,研究者逐渐发现,传统“代谢产物驱动的化学腐蚀”理论难以充分解释多类MIC现象,大量研究表明胞外电子传递(extracellular electron transfer, EET)在多种腐蚀微生物中发挥关键作用。Lovley[7]和Nealson[8]团队基于地杆菌Geobacter与希瓦氏菌Shewanella的研究建立了EET的分子机制基础,揭示微生物可通过导电结构与多血红素体系实现固相电子传递。Widdel团队对嗜铁脱硫弧菌Desulfovibrio ferrophilus IS5的研究进一步指出,部分SRB亦能利用EET直接从金属铁表面获取电子[9-10],为电子传递型MIC的提出提供了重要的实验证据。基于这些进展,Little等在教材与综述中将MIC归纳为化学型(Chemical MIC, C-MIC)与电子型(Electrical, E-MIC)两类[11],对现代理论进行了体系化整理,使该分类框架在腐蚀科学与海洋工程领域得到广泛采用。 尽管现有MIC理论体系已较为成熟,但其认识主要基于浅海与近岸等常压环境。深海在压力、温度和营养结构上与浅海差异显著,相关研究多聚焦于微生物生态与代谢适应等生物学过程,然而,深海条件如何影响金属界面MIC的关键环节,如微生物活性、生物膜结构、代谢策略及界面电子传递等,仍缺乏系统认识[12]。这些极端条件可能重塑金属表面的电化学过程,使深海MIC呈现不同于浅海的腐蚀模式。 在海洋强国建设和深海装备制造业快速发展的背景下,深海微生物腐蚀防护技术已成为保障国家海洋权益、产业安全和装备可靠性的重要基础。因此,系统研究深海MIC的过程及其机制,不仅有助于揭示极端环境下的材料失效规律,也为深海工程材料优化、防护体系设计与服役可靠性评估提供科学依据,对推动我国深海技术发展具有重要战略意义。本文构建了深海 MIC 的概念框架(图 1),并从深海环境、微生物群落及金属材料界面过程三个维度,对相关研究进展进行了系统梳理。 图 1 深海MIC中环境、微生物与金属材料界面过程的耦合关系示意 近年来,研究人员从不同角度揭示了深海环境中微生物腐蚀现象的存在及其潜在机制。Zhai等[13]在西太平洋雅浦海沟约5772 m深处开展原位挂片实验,系统评估了钛合金、不同类型铝合金及铜合金等7类材料表面的微生物群落组成。结果发现,合金元素显著影响其附着微生物的结构与功能特征:钛合金表面富集多样性较高的互利共生型生物膜,无铜铝合金表面以硫单胞菌Sulfurimonas等寡营养适应菌为主,群落多样性最低,铜合金及含铜铝合金表面则富集了大量耐铜或可利用铜的菌属,如寡养单胞菌Stenotrophomonas、伯克霍尔德菌Burkholderia、卡巴列罗氏菌Caballeronia、副伯克霍尔德菌Paraburkholderia等。这些结果揭示了深海材料表面生物膜的显著差异性及其潜在腐蚀风险。 长期原位实验进一步表明,深海微生物能够显著加速金属腐蚀。新加坡团队在约1988 m的深海环境中对低碳钢链环进行了长达10年的原位暴露实验[14]。研究发现,链环表面出现了严重的局部腐蚀,其腐蚀坑深度和腐蚀速率(约200 µm·a⁻¹)均明显高于纯化学腐蚀预期。链环表面富集的微生物群落与周围沉积物显著不同,优势菌包括脱硫囊菌Desulfocapsa、脱硫弧菌Desulfovibrio和假脱硫弧菌Pseudodesulfovibrio等硫循环菌,其中Desulfocapsa可通过硫歧化代谢途径加速FeS等腐蚀产物的生成,而Desulfovibrio则利用金属表面产生的氢气作为电子供体进行硫酸盐还原。宏基因组和通量平衡分析进一步揭示了硫代谢在深海MIC中的关键作用。这项长期原位实验表明,深海环境中微生物与金属界面电化学过程的高度耦合,是材料加速腐蚀的关键驱动因素之一。 除了人工暴露实验外,深海沉船和人工结构物也为MIC研究提供了宝贵的原位观测对象。位于墨西哥湾1700~2000 m深处的二战沉船U-166等钢质残骸显示,在Deepwater Horizon石油泄漏事件发生后,其表面腐蚀速率显著增加,相关宏基因组与微生物生态分析表明,这一变化与沉船表面微生物群落的演替密切相关:外源碳源输入改变了原有群落结构,促进了铁氧化菌(如海深菌属铁氧化菌Mariprofundus ferrooxydans)和硫代谢菌(如Sulfurimonas)等腐蚀相关微生物的增殖[15]。进一步研究发现,沉船表面微生物群落与周围沉积物及水体存在显著差异,呈现明显的选择性富集效应[16]。宏基因组分析揭示这些群落富含与金属还原、硫循环以及电子传递等代谢功能相关的基因,可能通过电子传递、局部酸化及硫化物生成等途径,促进深海环境中金属的加速腐蚀。 除常规冷水环境外,热液区也为深海MIC提供了重要的生态场景。日本研究团队将基于Kuroko-ore(黑矿型硫化物矿石)构建的海底热液地球化学反应器布放于约1 km水深处,在深海原位条件下连续运行14.5个月。反应器内部形成了富含微生物的“胶状沉淀”(slime-like precipitates),研究人员随后将这些沉淀物带回实验室,并以零价铁为唯一电子供体,分别在37 °C、50 °C 和70 °C条件下开展腐蚀诱导实验[17],以系统解析温度梯度对腐蚀机制的选择性调控作用。结果显示:①37 °C时,腐蚀群落主要由具硫酸盐还原能力的厚壁菌门(SRB-like Firmicutes)主导,可使铁的腐蚀速率提升约50倍。②50 °C时,出现产甲烷菌单独诱导的腐蚀,以及产甲烷菌-SRB协同腐蚀两种机制。③70 °C时,腐蚀主要由化学过程驱动。虽然热球菌Thermococcus、乳杆菌Lactobacillus等热适应微生物占优势地位,但其对铁溶解的促进效应有限,仅为无菌对照的 2~8倍,未表现出显著的微生物腐蚀效特征。群落分析结果显示,在所有易腐蚀样品中,厚壁菌门Firmicutes、广古菌门Euryarchaeota、变形菌门Proteobacteria和浮霉菌门Planctomycetota共占总丰度的90%以上,而传统海洋SRB丰度极低(<1.3%)。这说明热液环境中的深海MIC并非由典型SRB主导,而可能由产甲烷菌与部分产孢性厚壁菌驱动。 尽管来自不同深海场景的研究均揭示了深海微生物在金属腐蚀中的关键作用,但微生物的实际腐蚀贡献仍难以定量区分,尤其是有无微生物参与条件下材料腐蚀行为的差异缺乏系统原位评估。针对这一问题,研究人员提出结合耐压罐与0.22 μm微孔滤膜的原位对照装置[18]:通过微孔滤膜在深海构建“无外源微生物”暴露条件,实现与天然生物膜环境的直接对比(图2)。该方法为定量解析深海环境中微生物的腐蚀贡献提供了新的技术途径。未来,可进一步发展标准化的耐压有/无微生物对照腐蚀罐,以实现跨海域、跨材料体系的腐蚀贡献量化,并为深海腐蚀风险评估与防护策略制定提供关键依据。 a. 金属腐蚀罐;b. 金属腐蚀罐挂样现场;c. 有/无微生物金属腐蚀罐概念图 图2 基于滤膜过滤构建的无外源微生物对照金属腐蚀装置 深海环境最具代表性的理化特征是极高的静水压力, 这也是导致深海与浅海MIC差异的关键因素。新加坡南洋理工大学团队[19]构建了可控高压微生物腐蚀模拟装置,分别在 0.1 MPa、15 MPa与30 MPa 三个压力下,对比了常压环境分离的SRB(阿拉斯加脱硫弧菌Desulfovibrio alaskensis、嗜铁脱硫弧菌Desulfovibrio ferrophilus)与深海环境分离的SRB(假脱硫弧菌属深部菌Pseudodesulfovibrio profundus、假脱硫弧菌属嗜压菌Pseudodesulfovibrio piezophilus)的腐蚀行为。结果显示,深海来源的SRB在高压下的最大点蚀速率显著高于常压菌株;其中 P. piezophilus即使在30 MPa下仍具有强腐蚀能力。 最新的蛋白组学研究揭示了两株SRB对压力响应的分子基础[20]。嗜压型P. profundus缺乏外膜细胞色素等关键胞外电子传递组件,无法进行E-MIC,主要依赖乳酸氧化-硫酸盐还原产生H₂S的化学型C-MIC。随压力升高,其能量代谢适度增强,因而腐蚀能力略有提升。相反,常压型D. ferrophilus在0.1~15.0 MPa范围内通过富集铁硫蛋白与细胞色素构建有效的EET体系,实现强烈的E- MIC。但在30 MPa下,电子传递与能量相关蛋白显著下调,导致E-MIC能力衰减,腐蚀速率下降一个数量级。该研究表明,深海MIC的强度不仅取决于微生物代谢类型,更受其对压力的生理适应策略所决定。 高静水压会与SRB的代谢活动形成协同放大效应,使微生物诱导的点蚀更易演化为应力腐蚀开裂(stress corrosion cracking,SCC)。研究采用慢应变速率试验(slow strain rate test,SSRT)与原位电化学测试,在0.1-10 MPa条件下系统评估了典型SRB脱硫弧菌(Desulfovibrio desulfuricans)对X80管线钢SCC的影响[21]。相关研究表明,高压使得SRB对X80 管线钢造成的点蚀深度与密度均显著增加,显著降低裂纹形核的临界条件。SRB代谢生成的FeS类腐蚀产物在高静水压下表现出更强的阴极催化效应,既促进析氢反应,又抑制氢原子复合,从而显著增强氢的滞留与渗透。随之而来的氢在裂尖富集会进一步削弱材料局部韧性,使早期点蚀更易向脆性裂纹演化。与此同时,高静水压本身也提升了氢析出反应的热力学与动力学驱动力,进一步放大氢脆效应。二者叠加构成深海环境中“点蚀形核—氢脆扩展”失效路径的核心机制。 最新研究进一步揭示了深海流体动力与静水压力对MIC行为的影响。Ivanovich等[22]采用可控温压—流动高压生物电化学反应器,系统比较了P. profundus在流动与静态条件下的生物膜特征与腐蚀行为。结果显示,流动环境能够保持较高的活性细胞比例,显著增强界面电化学腐蚀能力;静态条件下形成的生物膜虽然生物量更高,但因代谢产物积累和营养扩散受限,死亡细胞比例上升、代谢活性下降,从而表现出相对较低的腐蚀活性。在0.1~30.0 MPa范围内,静水压力对P. profundus的代谢与腐蚀速率影响有限。总体来看,流体动力对腐蚀性生物膜结构与MIC行为的调控作用显著,静水压力则主要影响细胞附着等早期过程,二者共同塑造了深海环境下的 MIC 特征。 综上所述,深海MIC的形成与演化受静水压力、流体动力条件以及微生物腐蚀模式的共同调控。深海环境中特有的压力适应性、代谢状态和界面流动条件可能以不同于浅海体系的方式影响金属界面过程。因此,深海MIC的风险评估与机制推断必须综合考虑上述因素,而不能简单以浅海规律外推。 深海MIC的机制解析高度依赖于嗜压/耐压功能菌株的分离与其原位条件下的生理生态研究。关于深海嗜压微生物的系统探索可追溯至 ZoBell等[23-24]在20世纪中期的开创性研究,他们首次揭示了高静水压对海洋细菌生长与代谢的影响,为深海微生物学奠定了实验基础。随着高压采样与培养技术的进步,Yayanos等[25]于1979年首次从北太平洋深海分离出兼性嗜压菌株深部发光杆菌Photobacterium profundum CNPT-3,并系统揭示了其对高静水压的生长响应,被视为深海嗜压微生物研究的重要里程碑式。随后在1981年,该团队又从马里亚纳海沟分离出专性嗜压菌株MT-41[26],为后续的高压依赖性生理研究奠定了基础。Yayanos、Deming等[27-29]进一步从生理生化层面揭示了嗜压菌在细胞膜脂质流动性调节与胞外酶活性与能量代谢等方面的压力响应规律,初步构建了嗜压微生物学的经典理论框架。 近年来,深海微生物学研究经历了从资源获取到机制解析的范式转变。在技术层面,多通道高压培养系统与原位保压取样器的突破[30-31],不仅大幅提升了对嗜压菌生长动力学的模拟能力,还将研究范围从单一菌种拓展至冷泉、热液等复杂生态系统中的异养类群与古菌[32]。在分子层面,以P. profundum SS9为代表的模式嗜压菌株基因组被解析,系统揭示了压力适应所涉及的膜脂重构、核糖体结构调控及呼吸链改组等关键分子机制 [33-34]。 尽管近年来,热液、冷泉及富营养沉积物等生态系统中已分离出大量嗜压微生物,但针对腐蚀的定向菌株分离与鉴定工作仍十分有限。现有分离策略多以硫循环、产甲烷或铁还原等地球化学过程为导向,较少以金属腐蚀效应为筛选目标,导致深海环境尚未形成系统的腐蚀功能菌资源库。即便是已从深海获得的典型功能菌,如Desulfovibrio、Pseudodesulfovibrio、Shewanella和Methanococcus(甲烷球菌),其研究多局限于常压悬浮或沉积物体系,缺乏“高静水压—金属界面”耦合条件下对腐蚀效应的系统测试,难以建立代谢特征与腐蚀速率之间的真实对应关系从而限制了深海MIC机制的真实解析。 另一方面,深海微生物群落长期处于高静水压环境,采样过程中发生的减压与温度波动易导致优势功能群丢失及兼性快速生长菌的假性富集,从而偏离金属界面的真实群落特征。为评估采样方式对群落保真度的影响,He等[35]在南海1038 m深度比较了4种采样策略在群落组成、物种丰度分布及核酸保存稳定性方面的差异取样方案,重点分析了原位过滤及是否即时固定对群落代表性的影响。所采用的采样策略包括多通道原位核酸采集系统(multiple in situ nucleic acid collection, MISNAC)、原位过滤并固定(in situ microbial filtration and fixation, ISMIFF)系统、原位过滤未固定(in situ microbialfiltration without fixation, ISMIFU)系统以及传统的Niskin瓶采样系统。研究结果显示,原位核酸采集或即时固定的样品更能保持原位群落结构,而 Niskin瓶采样则显著富集 交替单胞菌Alteromonadaceae和嗜油菌Oleibacter等快速增殖菌,反映出明显的减压与升温扰动效应。在基因表达层面,原位固定样品中碳、氮、硫循环相关基因仍维持正常表达;而Niskin瓶采集的样品则以环境胁迫及运动能力相关的双组分调控系统(two component system, TCS)基因为主,表现出典型的应激特征。此外,ISMIFU系统采集的样品中大部分核心基因表达缺失,进一步凸显了RNA在非固定条件下会快速降解,原位固定或裂解是获得高保真MIC群落数据的前提。 最近的保压研究表明,深海微生物的功能验证高度依赖压力保真。Cao等[36]在马里亚纳海沟10903 m深处采用保压采样、等压转移和等压酶活性测定技术,对比了常压与原位压力下的胞外酶活性。结果显示,在 6000–10903 m 范围内,高静水压下的微生物胞外酶活性显著高于常压条件,其中β-葡萄糖苷酶的保压活性可达释压条件下的27倍。说明深渊带微生物的代谢体系在高压下并非普遍受抑,而是呈现明显的深度依赖型激活。对于腐蚀相关的代谢途径(如硫酸盐还原、金属还原等)而言,这种压力依赖性意味着,若在常压下进行功能测定,将不可避免地低估其在深海环境中的真实活性。 Cario等[37]通过比较传统静态高压容器(需反复释压/再加压)与等压浮动活塞装置(Pressurized Underwater Sample Handler, PUSH)对深海SRB菌株 Desulfovibrio salexigens(嗜盐脱硫弧菌)和极端嗜热古菌Archaeoglobus fulgidus(辉煌古球菌)生长动力学的影响,发现在全程保持压力的等压条件下,两种菌的生长速率显著提高,且指数生长期的耐压上限明显拓宽(D. salexigens 从20 MPa 提升至30 MPa,A. fulgidus 从 50 MPa提升至60 MPa),在≥30 MPa(或≥50 MPa)的高压区,循环释压导致明显的细胞死亡数,而等压培养仍能维持细胞缓慢生长。此外,经历多次释压后的细胞在转至常压培养时恢复能力显著下降。研究表明,传统的静态高压培养方法会系统性低估高压微生物的生长性能,因此在深海MIC研究领域引入等压采样、富集和培养技术,对于准确评估高压环境下的微生物真实生理活性至关重要。 近年来的研究不断深化了对深海MIC的认识,显示其形成过程受高静水压、流体动力条件及微生物的压力适应型代谢特征共同调控。深海环境中的微生物群落具有高度的环境选择性,不同地球化学背景下的功能群呈现差异化的腐蚀作用模式,而高压条件下,常压与嗜压菌株在电子传递策略、代谢路径及腐蚀能力方面表现出显著差异。这些结果表明,深海 MIC 是由“压力适应性-代谢特征-界面过程”耦合驱动的体系化腐蚀模式。 然而,深海 MIC 的机制解析仍受到关键技术条件的限制,主要体现在三个方面。其一,深海腐蚀功能菌株极度匮乏。尽管深海环境已分离出大量嗜压或耐压微生物,但能够在高静水压下进行腐蚀功能验证的菌株仍非常有限,严重制约了腐蚀机制的构建。其二,现有高压模拟平台难以复现深海“多因子耦合”界面条件。 虽然已有多类保压培养与等压转移装置(如 PUSH 系统、高压浮动活塞反应器等),但多数设备难以同时实现保压采样—等压转移—等压培养与流体剪切、营养供给、电化学监测等深海 MIC 所需的关键要素,使实验条件与真实深海界面过程仍存在显著差距。其三,深海样品在采集与转运过程中易受到减压与温度波动的影响,引发群落结构偏移和功能丢失,从源头上影响腐蚀机制的可靠解析。因此,突破深海 MIC 的研究瓶颈亟需建立从保压采样、菌株富集、等压培养到功能验证的高压全链条技术体系,为深海环境中微生物腐蚀行为的准确评估与机制解析提供可靠技术基础。 未来,深海 MIC 研究可从以下方向重点推进:① 构建高保真深海微生物获取体系:发展保压采样、原位过滤与即时固定技术,最大限度保持深海微生物的真实群落结构与瞬时代谢状态,为MIC研究提供可靠的微生物基础。② 建立连续、可控的深海高压腐蚀模拟平台:构建融合高静水压、温度/流速控制与原位电化学检测的深海模拟体系,实现对微生物生长、代谢通量与界面腐蚀过程的同步监测,获取深海环境下的真实腐蚀动力学数据。③ 建立深海腐蚀功能菌种资源库与标准化鉴定框架:系统分离并保存关键腐蚀功能菌株,明确其压力依赖代谢特征与腐蚀能力,实现 MIC 功能验证的可比性与可重复性。④ 构建高压条件下‘功能基因—代谢过程—腐蚀效应’的关联模型:融合高压转录组、蛋白组、代谢组与电化学/表面表征技术,建立驱动深海 MIC 的分子机制图谱,为腐蚀行为的预测与调控提供理论基础。⑤构建基于深海MIC机理的材料防护策略体系:基于深海环境中压力依赖的代谢与 EET 特征,开发耐压、抗生物膜或抑制电子传递的新型防护材料,实现从机理认知到工程应用的有效转化。 总体来看,深海 MIC 研究正处于由常压类比向压力依赖机制深化、由单点观测向系统集成研究演进的关键阶段。随着高压生物学、深海原位观测、高压腐蚀模拟、分子生态学与材料科学的持续交叉融合,未来有望形成面向深海环境的微生物腐蚀机制体系,并构建相应的风险评估与材料防护设计框架,为深海工程结构的长期可靠服役提供科学支撑。 [1] XU W, ZHANG R, DUAN J, et al. Corrosion is a global menace to crucial infrastructure: act to stop the rot now [J]. Nature, 2024, 629(8010): 41. [2] XU D, GU T, LOVLEY D R. Microbially mediated metal corrosion [J]. Nature reviews microbiology, 2023, 21(11): 705-718. [3] VON WOLZOGEN KÜHR C A H, VAN DER VLUGT L S. The graphitization of cast iron as an electrobiochemical process in anaerobic soil [J]. Water, 1934, 18:147-165. [4] ZOBELL C E. The effect of solid surfaces upon bacterial activity [J]. Journal of bacteriology, 1943, 46(1): 39-56. [5] DEXTER S C,GAO G Y. Effect of seawater biofilms on corrosion potential and oxygen reduction of stainless steel [J]. Corrosion, 1988, 44(10): 717-723. [6] HAMILTON W A. Sulphate-reducing bacteria and anaerobic corrosion [J]. Annual review of microbiology, 1985, 39: 195-217. [7] LOVLEY D R, PHILLIPS EJP. Rapid assay for microbially reducible ferric iron in aquatic sediments [J]. Applied and Environmental Microbiology, 1987, 53(7): 1536-1540. [8] MYERS C R, NEALSON K H. Bacterial manganese reduction and growth with manganese oxide as the sole electron acceptor [J]. Science, 1988, 240(4857): 1319-1321. [9] DINH H, KUEVER J, MUßMANN M. et al. Iron corrosion by novel anaerobic microorganisms [J]. Nature 2004, 427: 829-832. [10] ENNING D, GARRELFS J. Corrosion of iron by sulfate-reducing bacteria: new views of an old problem [J]. Applied Environmental Microbiology, 2014, 80(4):1226-36. [11] LITTLE B J, LEE J S. Microbiologically influenced corrosion [M]. Hoboken: Wiley-Interscience, 2007. [12] GE Y, WANG C, ETIM IN, et al. Deep-sea microbially influenced corrosion and biomineralization [J]. Frontiers in Microbiology, 2025, 16:1605909. [13] ZHAI X, CAO W, ZHANG Y, et al. Study on the bacterial communities of the biofilms on titanium, aluminum, and copper alloys at 5,772 m undersea in yap trench [J]. Frontiers in microbiology, 2022, 13: 831984. [14] RAJALA P, CHENG D Q, RICE S A, et al. Sulfate-dependant microbially induced corrosion of mild steel in the deep sea: A 10-year microbiome study [J]. Microbiome, 2022, 10(1): 4. [15] MUGGE R L, BROCK M L, SALERNO J L, et al. Deep-sea biofilms, historic shipwreck preservation and the Deepwater Horizon spill [J]. Frontiers in marine science, 2019, 6: 48. [16] HAMDAN L J, HAMPEL J J, MOSELEY R D, et al. Deep-sea shipwrecks represent island-like ecosystems for marine microbiomes [J]. The ISME journal, 2021, 15(10): 2883-2891. [17] WAKAI S, SAKAI S, NOZAKI T, et al. Accelerated iron corrosion by microbial consortia enriched from slime-like precipitates from a corroded metal apparatus deployed in a deep-sea hydrothermal system [J]. Microbes and environments, 2024, 39(5): ME23089. [18] 李程鹏. 基于宏基因组学研究海洋生物膜病毒多样性及对腐蚀微生物的影响机制[D/OL]. 青岛: 中国科学院海洋研究所, 2025. [19] YEO Y P. Molecular ecology and physiology of microbiologically-influenced corrosion in the deep sea [D/OL]. Singapore: Nanyang Technological University, 2024. [20] IVANOVICH N, GUO X, SOBOTA RM, et al. Adaptation to hydrostatic pressure modulates proteome dynamics in corrosive sulfate-reducing bacteria [J]. Microbiology Spectrum, 2025, e0159025. [21] LI J, ZHOU E, XIE F, et al. Accelerated stress corrosion cracking of X80 pipeline steel under the combined effects of sulfate-reducing bacteria and hydrostatic pressure [J]. Corrosion science, 2025, 243: 112593. [22] IVANOVICH N, MARSILI E, SHEN X, et al. Exploring the impact of flow dynamics on corrosive biofilms in the deep-sea with high-pressure bio-electrochemostasis [J]. Frontiers in microbiology, 2025, 16:1540664. [23] ZOBELL C E, JOHNSON F H. The influence of hydrostatic pressure on the growth and viability of terrestrial and marine bacteria [J]. Journal of bacteriology, 1949, 57(2): 179-189. [24] ZOBELL C E, OPPENHEIMER C H. Some effects of hydrostatic pressure on the multiplication and morphology of marine bacteria [J]. Journal of bacteriology, 1950, 60: 771-781. [25] YAYANOS A A, DIETZ A S, VAN BOXTEL R. Isolation of a deep-sea barophilic bacterium and some of its growth characteristics [J]. Science, 1979, 205(4408): 808-810. [26] YAYANOS A A, DIETZ A S, VAN BOXTEL R. Obligately barophilic bacterium from the Mariana trench [J]. Proceedings of the National Academy of Sciences, 1981, 78(8):5212-5. [27] HUSTON A L, DEMING J W. Relationships between microbial extracellular enzymatic activity and suspended particulate matter in the North Water Polynya, North Water Polynya Study [J]. Deep Sea Research Part II: Topical Studies in Oceanography, 2002, 49(22-23): 5211-5227. [28] DEMING J W. Psychrophiles and polar regions [J].. Current Opinion in Microbiology, 2002, 5(3), 301-309. [29] DELONG E F, YAYANOS A A. Adaptation of the membrane lipids of a deep-sea bacterium to changes in hydrostatic pressure [J]. Science, 1985, 228(4703): 1101-1103. [30] YAYANOS A A. Deep-sea piezophilic bacteria [J]. Methods in Microbiology, 2001, 30: 615-637. [31] KATO C, LI L, NOGI Y, et al. Extremely barophilic bacteria isolated from the Mariana Trench, Challenger Deep, at a depth of 11,000 meters [J]. Applied Environmental Microbiology. 1998, 64(4):1510-3. [32] MARTEINSSON V T, BIRRIEN J L, REYSENBACH A L, et al. Thermococcus barophilus sp. nov., a new barophilic and hyperthermophilic archaeon isolated under high hydrostatic pressure from a deep-sea hydrothermal vent [J]. International Journal of Systematic Bacteriology, 1999, 49(2):351-9. [33] VEZZI A, CAMPANARO S, D'ANGELO M, et al. Life at depth: Photobacterium profundum genome sequence and expression analysis [J]. Science. 2005, 307(5714):1459-61. [34] BARTLETT D H. Pressure effects on in vivo microbial processes[J]. Biochimica et Biophysica Acta (BBA), 2002, 1595(1-2): 367-381. [35] HE Y, ZHANG H, BALTAR F, et al. Transcriptional difference of deep-sea microorganisms under different sampling methods [J]. Environmental science & technology, 2025, 59(23): 11653-11665. [36] CAO J, WANG J, ZHANG H, et al. Isobaric enzymatic assays reveal depth-dependent variation in microbial ectoenzyme activities in the deepest ocean on earth [J]. Science China earth sciences, 2025, 68(1): 185-194. [37] CARIO A, GROSSI V, SCHAEFFER P, et al. Membrane homeoviscous adaptation in the piezo-hyperthermophilic archaeon Thermococcus barophilus [J]. Frontiers in Microbiology, 2015, 6: 1152. 





免责声明:本网站所转载的文字、图片与视频资料版权归原创作者所有,如果涉及侵权,请第一时间联系本网删除。

官方微信
《腐蚀与防护网电子期刊》征订启事
- 投稿联系:编辑部
- 电话:010-62316606
- 邮箱:fsfhzy666@163.com
- 腐蚀与防护网官方QQ群:140808415