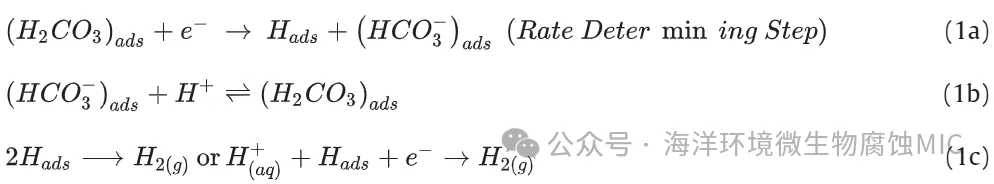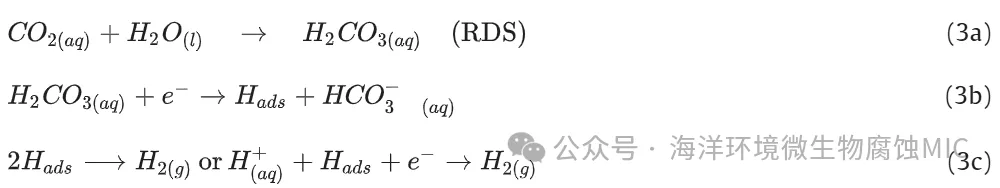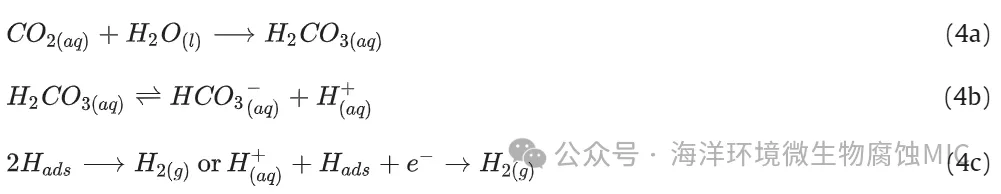在 CO2 水环境中碳钢的腐蚀仍然是油气系统中的一个关键挑战。尽管经过数十年的研究,CO2 的机制作用仍然是一个争论的话题。在本研究中,在 0.17 mol L⁻1 NaCl 溶液中,于 pH 3–5 条件下,在 CO2 饱和和 N2 吹扫两种条件下系统地进行了电化学阻抗和极化测量。结果表明,CO2 腐蚀速率与 pH 无关,这与 N2 系统不同,在 N2 系统中,腐蚀随酸度增加而增加。阻抗图揭示了一个特征性的感抗环,其频率在 CO2 条件下不随 pH 变化,这被解释为水合 CO2 物种的催化作用。开发了一个新的电化学模型,除了经典的缓冲机制外,还引入了这种催化作用在析氢反应中的作用。该新模型定量地再现了 pH 无关的腐蚀速率和阻抗响应,从而在碳钢 CO2 腐蚀的机制框架中迈出了重要一步。
研究 CO2 腐蚀机理的需求源于观察表明,在碳酸环境中脱气溶液对碳钢的腐蚀性比相同 pH 值的酸更强。理解 CO2如何影响腐蚀机理对于改进预测腐蚀速率的模型至关重要,同时也有助于开发缓解石油和天然气行业系统腐蚀的策略。关于 CO2腐蚀的研究,始于 1975 年,当时 De Waard 和 Milliams将 CO2归因于碳钢腐蚀机理中的阴极作用。
1975 年,De Waard 和 Milliams首次提出了一种涉及碳酸的额外阴极反应(公式 1a),以解释含有 CO2的水溶液中腐蚀速率的增加。
对于所提出的机制( 公式 1a、1b 和 1c),需要做出若干假设,才能定量解释与实验确定的腐蚀速率结果相匹配。尽管这一方法在历史上具有重要意义,但当前的知识揭示了该模型存在若干局限性。尽管如此,它仍然成为该介质中最广泛使用的机制。
在接下来的几十年里,关于 CO2 腐蚀的多种研究在其机制中都考虑了某种形式的碳酸还原反应。那些假设存在一种涉及碳酸还原的额外阴极反应的研究被称为直接还原机制。
其中一篇被高度引用的论文是 Schmitt 和 Rothmann 在 1977 年的研究。除了讨论直接还原反应外,他们还引入了一种化学反应——吸附 CO2 的水合反应——作为 CO2 腐蚀阴极机制中的速率控制步骤(RDS)((2a), (2b), (2c), 和 2d)。
施密特和罗特曼是最早利用旋转圆盘电极来建立良好控制的水动力学条件的研究者之一。他们基于列维奇提出的扩散边界层概念开展了研究。他们的研究结果揭示了二氧化碳水合在 CO2 腐蚀过程中起着关键作用。作者在该过程中识别出两个成分:一个与 H+ 离子和 H2CO3的扩散相关,另一个成分与扩散无关。后者仅存在于水溶液中的 CO2,与吸附的 CO2 在电荷转移步骤之前的非均相反应有关。
1983 年,Wieckowski 等人利用放射性碳的示踪方法,研究了碳酸盐类物质在铁表面的潜在吸附过程。他们的研究发现,在自由铁表面未检测到碳酸盐类物质,从而否定了 Schmitt 和 Rothmann 提出的模型。到 20 世纪 80 年代末,Gray 等人在 Wieckowski 等人工作的基础上,提出了一个值得注意的假设。他们提出,溶解的 CO2 的水合过程并非在吸附状态下发生,而是在均相条件下进行(详见 (3a)、(3b) 和 3c)。
格雷等人推导出了一个由 CO2 缓慢水合控制的极限电流解析表达式,利用了利维奇提出的扩散边界层和反应层概念。他们将这些发现纳入一个定量模型。20 世纪 90 年代,内西克等人的研究也假设了 H2CO3 的电化学还原和溶解 CO2 的均相水合反应的存在。1999 年,林特和伯斯坦的工作带来了完全不同的视角。他们挑战了涉及 H2CO3 还原的额外阴极反应的概念。作者们通过定性分析得出结论,含有溶解 CO2 的缓冲溶液可以完全解释在相同 pH 值的酸性溶液中测得的钢的阴极电流增加现象。他们将这种现象归因于碳酸的解离,碳酸作为 H+ 离子的储存库——阴极反应的前体,正如 [4a]、[4b] 和 4c 所示。
后来,在 2008 年,Remita 等人对含有溶解 CO2 的水溶液的缓冲效应进行了定量研究,并探讨了其对整体阴极电流的贡献。他们通过理论计算、钢旋转圆盘电极的测量以及界面 pH 测量来支持缓冲效应的机制。这项工作证实了 Linter 和 Burstein的定性观察。在此基础上,Tran 等人在 2015 年确认了这些发现。他们采用了一种与考察乙酸对阴极机制影响的研究类似的实验方法。在该研究中,他们使用了与碳钢相似的阴极分支的不锈钢,从而消除了阳极反应的干扰。作者观察到,CO2 分压的增加并未影响电荷转移电流。 他们提到缓冲效应机制占主导地位,指出主要的阴极反应涉及 H+ 离子的还原,因为直接还原机制未被检测到。自那以后,文献中并未报道有关阴极机制理解的进一步进展。 后续研究,包括 Kahyarian 等,支持了 Tran 等关于缓冲效应机制的假设。
CO2 对碳钢腐蚀机制中阳极反应的影响,通常通过 Bockris 等人提出的模型进行考察。该模型最初是为缺乏 CO2的酸性环境开发的。尽管 Heusler提出了一个更全面的模型,能够描述稳态和瞬态行为,但 Bockris 模型在文献中仍然广泛使用。这一点尤其体现在关于 40 mV(Bockris)和 30 mV(Heusler)的 Tafel 斜率的讨论中。许多研究人员在没有充分评估模型选择时 40 mV 斜率和 10 mV 差异的物理意义的情况下,选择了使用 40 mV 斜率。此外,如后文所述,Tafel 斜率不应被视为建立反应模型的可靠标准。尽管存在这些局限性,Bockris 模型仍然被应用于含有 CO2的环境,作者在多项研究中报告了相同的 40 mV 塔菲尔斜率。直到 20 世纪 70 年代,I. Epelboin 和 M. Keddam才引入了电化学阻抗的系统性应用,这是一种瞬态技术,用于研究酸性条件下铁的溶解机制。由于电化学阻抗具有线性特性,因此在研究电化学动力学方面具有显著优势,允许进行数学线性分析。 然而,尽管阻抗已成为探索电化学动力学的一种有价值工具,许多腐蚀机制研究仍仅依赖稳态技术。这些方法的显著局限性在于,多种模型往往能与收集到的静止数据相吻合,导致难以区分机制解释,包括阴离子的影响。
长期以来,即使在含 CO2 的介质中,铁的阳极溶解机制被认为遵循 Bockris 等人提出的模型。然而,1996 年,Nesic 等人挑战了 CO2 对阳极过程没有影响的观点。他们根据研究结果提出了新的反应级数和 Tafel 斜率,并为三个不同的 pH 范围提出了具体的反应机制。他们介绍的第一个反应,如式 5 所述,涉及一种新的平衡,其中含碳物种吸附在铁表面。这种物质将作为由该反应引发的铁溶解的中间体。
此外,基于 pH 值小于 4 的稳态数据提出了五个基元步骤,对于 pH 值在 4 到 5 之间的提出了五个额外的步骤,而对于 pH 值大于 5 的提出了五个进一步的步骤。这些步骤集中的每一个都以公式 5 开始。作者还指出,与相同 pH 值的强酸溶液相比,二氧化碳溶液中铁的溶解动力学不同,这与一种作为化学配体的碳酸物种有关,该物种促进了铁的溶解。
2017 年,Almeida 等人通过研究先前报道的碳钢自由表面(FeCO2)ads的形成,探讨了 CO2 在碳钢自由表面的潜在作用。作者采用了电化学阻抗技术,并开发了一种消除除 H2O–CO2 系统产生的阴离子之外任何阴离子干扰的方法,同时施加高达 30 bar 的 CO2 压力。他们对实验结果的分析以及阻抗计算表明,CO2 不会直接影响自由铁表面,从而排除了(FeCO2)ads 形成的假设。
Kahyarian 等通过塔菲尔斜率分析,提出二氧化碳(CO2)在碳钢的溶解机制中起阳极作用。Almeida 等对此主题进行了详细讨论,指出了 Kahyarian 等所用方法的局限性。他们的分析完全依赖塔菲尔斜率来得出 CO2 参与阳极机制的结论。他们观察到塔菲尔斜率从 28 mV 降至 22 mV,并将其用于支持其关于 CO2 参与阳极反应的假设。引用了 6 mV/decade 的塔菲尔斜率差异,以确认 CO2 在碳钢阳极反应中的作用。
尽管已经证明 CO2 不能直接作用于自由铁表面形成(FeCO2)ads,并且考虑到仅基于稳态数据分析的脆弱性,正如 Kahyarian et al.所进行的分析那样,对于作者们来说,问题仍然是 CO2 是否可能对碳钢的阳极溶解机制产生某些影响。
2024 年,Moradighadi 等人等旨在通过在多种阳极电位下引入电化学阻抗测量,进一步阐明腐蚀机制。这项研究受到 Keddam 等人关于酸性介质中铁溶解工作的启发。实验方法重点研究了存在和不存在 CO2 时的腐蚀机制。在无 CO2 的介质中,铁溶解速率的变化由氯离子和氢氧根离子在铁表面竞争吸附的假说解释。这种竞争导致形成含氯中间物种。尽管这一观点与 Barcia 和 Mattos报告的发现形成鲜明对比,但这些差异的详细讨论超出了本文的范围,并将在未来加以探讨。 在饱和 CO2 的环境中,Moradighadi 等支持了 Almeida 等的发现,指出阳极机制与 Keddam 等为强酸性溶液中铁的阳极溶解过程提出的机制保持一致。然而,对氯化物溶液中阳极稳态动电位扫描曲线的定性分析使作者认为,与相同 pH 值的完全电离酸相比,CO2 饱和水环境中的铁溶解动力学更大。 因此,这些发现回归到先前讨论的稳态数据的解释,这些数据不能作为定义特定机制的论据。
这项对文献的历史分析表明,尽管对于缓冲机制在阴极反应中的作用存在普遍共识。为了阐明涉及 CO2 的腐蚀过程,阴极和阳极过程都需要进一步研究。然而,现在已经确定,在腐蚀电位下,CO2 不起阳极作用。
这项研究通过电化学阻抗和极化曲线在 pH 值 3 至 5 范围内进行的系统考察,展示了关于 CO2 腐蚀过程的新发现。这些新结果通过一种先前未建立的新基本反应得到解释,该反应展示了水合 CO2 物种诱导的催化行为。
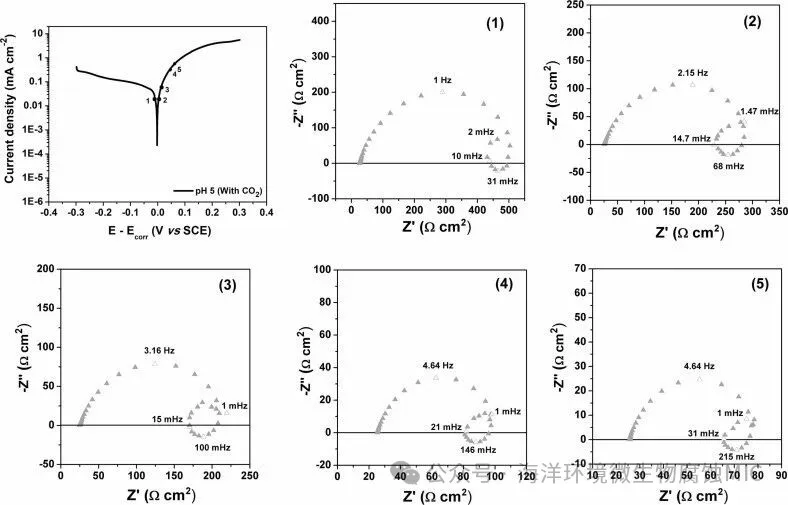
在饱和 CO2 的 NaCl 溶液(0.17 mol L⁻1)中 pH 5 时的阻抗图。阻抗测量所进行的极化点用数字标出:(1) -7 mV;(2) +7 mV;(3) +15 mV;(4) +38 mV;(5) +51 mV。Ecorr = -0,721 V。
本研究中的所有阻抗图均表现出三个时间常数。这导致在高频范围内出现一个电容响应,与双层弛豫相关,随后在低频范围内出现一个电感响应和另一个电容响应。在pH=5中,一个重要观察是电感回路的特征频率对所有测量的阻抗都保持恒定,约为 4.6 mHz。在 pH=4,阻抗图中的电感回路特征频率在所有选定点(包括阳极和阴极分支)始终保持在 10 mHz。同样,在 pH=3,电感回路特征频率在施加电流密度的整个范围内保持恒定,约为 21 mHz。该频率是 pH=4 时观察到的频率的两倍,表明在 pH 值较低的系统中动力学更快。此外,随着 pH 值的降低,第一个电容回路的直径减小,这与更腐蚀性的环境相符。 在开路电位下测得的电荷转移电阻(RCT)对于腐蚀性较弱的 pH=5 时,约为 5000-ohm cm2。这种电阻在 pH=4 时下降至约 2000-ohm cm2,并在 pH=3 时达到约 400-ohm cm2。
对于饱和 CO2 的系统,在 pH=5 时,无论施加的电流密度如何,都观察到相同的三个循环。与存在 N2 时感应循环的频率保持不变不同,引入 CO2 导致在施加电流密度的范围内出现明显的频率偏移。在阳极方向,频率增加。然而,与 N2 的行为不同,pH 的降低并未导致感应循环特征频率的增强。电荷转移电阻(RCT)表明,当存在 CO2 时,腐蚀更为剧烈,约为 200-ohm cm2。
免责声明:本网站所转载的文字、图片与视频资料版权归原创作者所有,如果涉及侵权,请第一时间联系本网删除。

官方微信
《腐蚀与防护网电子期刊》征订启事
- 投稿联系:编辑部
- 电话:010-62316606
- 邮箱:fsfhzy666@163.com
- 腐蚀与防护网官方QQ群:140808415